中药抗乙肝病毒活性及作用机制的研究进展
- 分类:医药文化
- 作者:伍 磊,张志鹏,蔡文涛,温海梅,陈 勇.中药抗乙肝病毒活性及作用机制的研究进展 [J]. 中草药, 2020, 51(24):6367-6376.
- 来源:伍 磊,蔡文涛 中草药杂志社
- 发布时间:2021-03-17 10:02
- 访问量:
【概要描述】
中药抗乙肝病毒活性及作用机制的研究进展
【概要描述】
- 分类:医药文化
- 作者:伍 磊,张志鹏,蔡文涛,温海梅,陈 勇.中药抗乙肝病毒活性及作用机制的研究进展 [J]. 中草药, 2020, 51(24):6367-6376.
- 来源:伍 磊,蔡文涛 中草药杂志社
- 发布时间:2021-03-17 10:02
- 访问量:
摘 要:乙肝病毒是一种能导致机体产生急性或慢性乙型肝炎(乙肝)的嗜肝性DNA病毒。乙肝现已成为全球性公共卫生疾病,易恶化发展为肝硬化、肝衰竭,甚至肝癌,严重威胁着人类的健康。中药及其活性成分发挥着重要的抗乙肝病毒活性,对中药抗乙肝病毒活性及其作用机制进行综述,以期为今后抗乙肝病毒研究提供一定的参考。
乙肝病毒是一种能导致机体产生急性或慢性乙型肝炎(乙肝)的嗜肝性DNA病毒。目前全球约有3.5%的人口感染慢性乙肝,慢性乙肝如未得到及时治疗,极易发展为肝硬化、肝衰竭,甚至肝癌,严重威胁人类的健康[1]。目前,临床常用的抗乙肝病毒药物主要有2类,即核苷(酸)类似物和干扰素。前者包括恩替卡韦、拉米夫定等药物,它们在长期用药过程中易导致机体产生耐药性且停药后会出现严重的反跳现象;而后者适应证窄、不良反应明显、需注射给药且价格昂贵[2]。因此,迫切需要开发出一些新型的抗乙肝病毒药物用于当前乙肝的治疗。
中药及其活性成分以其独特的优势发挥着重要的抗乙肝病毒作用,具有广阔的应用前景。笔者查阅了近5年中药抗乙肝病毒的相关文献,对中药抗乙肝病毒活性及作用机制的研究进展进行综述,旨在为今后抗乙肝病毒中药的研究提供参考。
1 单味中药活性成分抗乙肝病毒作用
1.1 茵陈
茵陈来源于菊科植物滨蒿Artemisia scopariaWaldst. et Kit.或茵陈蒿Artemisia capillaris Thunb.,具有清利湿热、利胆退黄的功效[3],其抗乙肝病毒活性成分主要有葡萄糖苷、倍半萜、绿原酸、对羟基苯乙酮、烯炔等。Geng课题组在肝癌HepG2.2.15细胞上考察了多种茵陈提取物的抗乙肝病毒活性,发现3种葡萄糖苷对乙肝病毒DNA的复制、乙肝病毒表面抗原(HBsAg)及乙肝病毒e抗原(HBeAg)的分泌均有很强的抑制活性,半数抑制浓度(IC50)均小于3.00 μmol/L;桉烷倍半萜对乙肝病毒DNA的复制、HBsAg和HBeAg的分泌均具有较强的抑制活性,IC50分别为12.01、15.02、9.00 μmol/L;绿原酸及其类似物、对羟基苯乙酮、烯炔等对乙肝病毒DNA的复制具有较强的抑制活性,IC50均小于15.00 μmol/L,而对HBsAg、HBeAg的分泌具有轻度的抑制活性[4-8]。上述茵陈提取物体外抗乙肝病毒活性显著,为进一步的机制研究和抗乙肝病毒药物研发奠定基础。
1.2 虎杖
虎杖采自于蓼科植物虎杖Polygonum cuspidatum Sieb. et Zucc.,具有利湿退黄、清热解毒、散瘀止痛等功效[3],其包含的抗乙肝病毒活性成分主要有槲皮素、白黎芦醇等。Cheng等[9]将槲皮素作用于HepG2.2.15细胞和pCH-9/3091(包含1.1倍乙肝病毒全基因组)转染的Huh7细胞后,HBsAg、HBeAg的分泌及乙肝病毒DNA的复制均受到明显的抑制,且此抑制活性在与拉米夫定、阿德福韦、恩替卡韦等合用时得到增强,作用机制可能与槲皮素下调热休克蛋白(heat shock protein,Hsp)40、Hsp70、Hsp90-β的表达,抑制乙肝病毒的转录有关。Parvez等[10]用槲皮素持续处理HepG2.2.15细胞5 d后,培养上清中HBsAg、HBeAg的分泌受到明显抑制,但继续处理则会造成细胞过度生长和死亡;分子对接结果显示,槲皮素与乙肝病毒聚合酶(polymerase,Pol)有较强的结合活性。Park等[11]用白黎芦醇处理能稳定表达乙肝病毒x蛋白(hepatitis B virus x protein,HBx)的Huh7-HBx细胞后,丝苏氨酸蛋白激酶(ser-ine-threonine protein kinase,Akt)信号转导受到干扰,细胞周期蛋白D1(cyclin D1)表达水平降低,使细胞增殖受到抑制;体内Huh7-HBx细胞异种移植小鼠模型也证实了白藜芦醇对肿瘤生长的抑制活性,提示白藜芦醇具有降低慢性乙肝病毒感染患者发生肝癌风险的潜在作用。然而,Shi等[12]报道,白黎芦醇可激活Sirt1-PGC-1α-PPARα信号轴,从而增强乙肝病毒核心启动子活性,进而促进乙肝病毒转录和复制,导致乙肝症状加重。文献报道白黎芦醇对乙肝病毒影响存在的两面性使得其能否成为抗乙肝病毒的活性化合物还有待进一步研究。
1.3 丹参
丹参来源于唇形科植物丹参Salvia miltiorrhiza Bge.的干燥根和根茎,具有良好的保肝护肝功效[3]。丹参素、迷迭香酸、紫草酸等为丹参主要的抗乙肝病毒活性成分。段树鹏等[13]研究发现HepG2.2.15细胞经丹参素处理后,乙肝病毒逆转录酶活性降低,使乙肝病毒DNA的复制受到直接的抑制作用,HBsAg、HBeAg的表达也随之受到抑制。Tsukamoto等[14]报道迷迭香酸对Hep38.7-Tet细胞和乙肝病毒感染的人原代肝细胞培养上清中乙肝病毒DNA的分泌具有显著的抑制作用,对其中HBsAg的分泌具有轻度的抑制作用,机制可能与干扰乙肝病毒前基因组RNA(pregenomicRNA,pgRNA)与Pol的结合有关。此外,笔者研究发现丹参中多酚类化合物紫草酸作用于HepG2.2.15细胞后,明显抑制乙肝病毒DNA的复制,其机制可能是紫草酸通过上调溶酶体膜相关蛋白1/2(lysosome-associated membrane proteintype1/2,LAMP1/2)、组织蛋白酶D(cathepsin D,Cath-D)的表达使得溶酶体的酸化功能增强以及通过抑制PI3K/Akt/ mTOR细胞信号通路来促进自噬体的形成,进而诱导肝细胞发生完整的自噬以干扰乙肝病毒复制。
1.4 苦参
苦参为豆科植物苦参Sophora flavescens Ait.的干燥根[3],其抗乙肝病毒活性成分主要包括苦参碱、氧化苦参碱、槐定碱等苦参碱型生物碱及苦参多糖等。冯静等[15]研究发现苦参碱对HepG2.2.15细胞中乙肝病毒DNA复制具有较强的抑制作用,机制可能与抑制Pol的活性有关;此外,它与拉米夫定合用能增强后者抗乙肝病毒的效果。张轩等[16]和Sang等[17]分别发现氧化苦参碱能明显抑制HepG2.2.15细胞培养上清和水动力注射pAAV-HBV 1.2小鼠血清中HBsAg、HBeAg的分泌及乙肝病毒DNA的复制。Chen等[18]报道槐定碱处理HepG2.2.15细胞72h后,HBsAg、HBeAg的分泌及乙肝病毒DNA的复制均受到明显的抑制,且抑制活性优于苦参碱和氧化苦参碱。Yang等[19]研究发现苦参多糖显著抑制HepG 2.2.15细胞HBsAg、HBeAg的分泌,机制可能与调控干扰素(interferon,IFN)-γ、白介素(interleukin,IL)-6和肿瘤坏死因子(tumornecrosis factor,TNF)-α等炎性细胞因子的分泌有关。
1.5 其他单味中药活性提取物
除上述单味中药提取物外,近年来还有一大批中药提取物被发现具有抗乙肝病毒活性,为抗乙肝病毒药物的开发提供了巨大的潜在活性化合物库。Parvez等[20]研究发现芦荟提取物芦荟大黄素抑制HepG2.2.15细胞HBsAg、HBeAg分泌及乙肝病毒的复制,作用机制可能与其抑制Pol活性有关;同时,研究结果显示芦荟大黄素对于乙肝病毒的抑制活性与拉米夫定相当,这可能与其活化细胞色素P450有关。笔者研究发现原儿茶酸通过激活ERK1/2信号通路介导的肝细胞核因子(hepatocytenuclear factor,HNF)-4α和-1α下调作用抑制乙肝病毒X启动子、核心启动子和前S1启动子,从而影响乙肝病毒的转录和复制[21];同时,原儿茶酸与拉米夫定联合应用能够显著增强两者对于乙肝病毒DNA、HBsAg、HBeAg等的分泌的抑制作用,且使两者的作用时间延长,同时起到良好的保肝作用[22]。
茵陈、虎杖、丹参、苦参等单味中药中的有效成分及提取物被报道具有抗乙肝病毒活性,见表1。
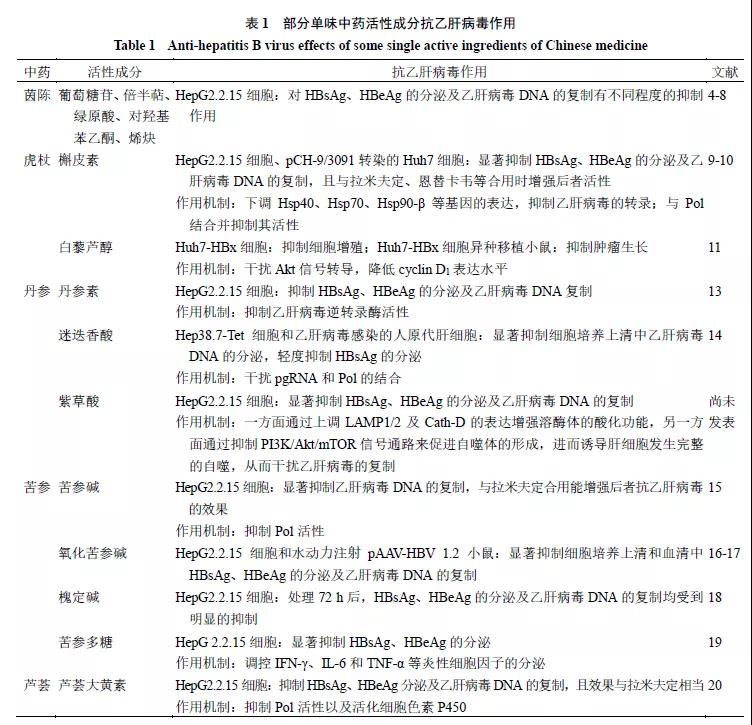
2 中药复方抗乙肝病毒作用
2.1 复方叶下珠
复方叶下珠是以叶下珠、黄芪、三七、甘草等组成的中药复方。Li等[23]报道复方叶下珠处理能稳定表达HBx的HepG2-HBx细胞和HepG2-HBx细胞移植小鼠后,HepG2-HBx细胞增殖、迁移、克隆形成及小鼠肿瘤的生长均受到了显著的抑制作用,其机制可能与HBx-SHH信号轴的失活有关,提示复方叶下珠具有降低乙肝向肝癌恶化的治疗潜力。Tong等[24]选择102例合并乙肝肝硬化再生或发育不良结节的乙肝患者作为研究对象,发现复方叶下珠能够在一定程度上抑制乙肝病毒DNA的复制,能预防或延缓乙肝病毒患者向肝癌方向恶化。谭本仁等[25]研究发现,复方叶下珠滴丸对HepG2.2.15细胞培养上清和HBsAg阳性患者血清培养液中HBsAg、HBeAg和乙肝病毒DNA复制均有一定程度的抑制作用。
2.2 小柴胡汤
小柴胡汤源于《伤寒杂论》,由柴胡、黄芩、人参、半夏、甘草、生姜、大枣7味中药组成[26]。李洁霞[27]报道小柴胡汤联合阿德福韦对乙肝患者有较好的疗效,且作用优于单独使用阿德福韦。陈少芳等[28]给临床慢性乙肝肝郁脾虚证患者应用加味小柴胡汤7 d后,取含药血清处理HepG2.2.15细胞,上清中HBsAg的分泌受到明显抑制。此外,万石川[29]研究发现加味小柴胡汤能够显著抑制HepG2.2.15细胞HBsAg、HBeAg的分泌,机制与其抑制JAK2-STAT3信号通路有关。
2.3 补肾复方
补肾复方是由黄芪、女贞子、淫羊藿、猫爪草、胡黄连、青皮6味中药组成的中药验方。Ji等[30]报道,在对恩替卡韦具有部分病毒学应答的患者中,HBeAg阳性乙肝患者在应用补肾复方联合恩替卡韦治疗后效果明显优于单独使用恩替卡韦,这可能与调节性T细胞(regulatoryT cells,Treg)比例的降低和树突细胞上细胞程序性死亡配体1(programmed death-L1,PD-L1)水平的下调相关。Li等[31]研究发现补肾复方能够降低HBeAg阳性乙肝患者血清中丙氨酸氨基转移酶(alanineaminotransferase,ALT)和乙肝病毒DNA的水平,对伴有ALT水平轻度升高的乙肝病毒患者有较良好的疗效,机制与其降低CD4+CD25+T细胞比率以及上调CD4+T细胞中IFN-γ表达水平的有关。同时,Li等[32]还发现了针对于单独应用恩替卡韦疗效不佳的乙肝患者,补肾复方联合恩替卡韦使用能改善HBsAg和HBeAg清除率等指标,提示补肾复方可作为恩替卡韦有效的补充药物。
2.4 扶正化瘀胶囊
扶正化瘀胶囊由丹参、桃仁、发酵虫草菌粉、松花粉、绞胶蓝、五味子6味中药组成。Wang等[33]报道扶正化瘀胶囊作为辅助治疗药物配合常规的抗乙肝病毒治疗方法,能更有效地调节乙肝病毒相关性肝硬化患者ALT、天冬氨酸氨基转移酶(aspartate aminotransferase,AST)、III型前胶原(PCIII)、透明质酸(hyaluronic acid,HA),层粘连蛋白(laminin,LN)等水平并提高乙肝病毒DNA转换率,且无严重的不良反应。Wu等[34]收集慢性乙肝并发肝硬化的患者外周血CD4+T细胞CD8+T细胞及自然杀伤细胞,与人肝星状细胞(hepatic stellate cell,HSC)系LX-2细胞体外共培养,并用刀豆蛋白A诱导慢性肝损伤,检测发现扶正化瘀胶囊显著提高自然杀伤细胞的比例、诱导LX-2细胞凋亡和坏死,下调α-平滑肌肌动蛋白和Ⅰ型前胶原的表达,提示扶正化瘀胶囊通过调节T淋巴细胞亚群的比例和功能来间接抑制HSC的增殖及活化,并促进HSC的凋亡和坏死,从而有助于阻断纤维化进程。
2.5 其他
除了上述中药复方之外,近年来随着对抗乙肝中药的深入研究,还有一大批中药复方的抗乙肝活性被报道。Kim等[35]研究发现由茵陈、地榆、姜黄组成的中药复方KCT-01能显著抑制HepG2.2.15细胞中HBsAg、HBeAg和病毒颗粒的分泌和pgRNA的合成,而不影响细胞活力;同时,能抑制乙肝病毒复制模型小鼠血清病毒粒子的产生及炎性细胞因子的合成,并降低小鼠肝细胞共价闭合环状DNA(covalentlyclosed circular DNA,cccDNA)水平;此外,KCT-01与恩替卡韦合用能增强后者体内、外抗乙肝病毒活性。Zhang等[36]报道温肾处方能够提高具有高基线ALT水平和肾阳虚证的慢性乙肝患者HBeAg血清学转换、乙肝病毒DNA转阴率及ALT正常化,且无严重不良反应。Zhao等[37]发现簕草石复方提取物可抑制鸭乙肝病毒感染鸭乙肝模型DHBsAg、DHBeAg和鸭乙肝病毒复制,且可降低ALT和AST水平,并改善鸭肝组织病变;同时,簕草石复方提取物也能抑制HepG2.2.15细胞HBsAg和HBeAg的分泌。
诸多中药复方被报道具有抗乙肝病毒活性,常见如表2所示。

3 中药抗乙肝病毒作用机制
目前中药抗乙肝病毒的作用机制主要涉及靶向病毒的直接途径和靶向宿主的间接途径2个方面,见图1。已报道中药的抗乙肝病毒主要机制分为直接途径(靶向病毒)和间接途径(靶向宿主)2大类。前者主要包括抑制乙肝病毒的侵入(如EGCG、水飞蓟宾、原花色素等)、靶向乙肝病毒cccDNA(如安石榴苷、姜黄素等)和抑制乙肝病毒转录(如柴胡皂苷C、黄芩苷、木犀草素等)等机制;后者主要包括调控乙肝病毒诱导的细胞自噬(如EGCG、腐殖酸等)、调控宿主免疫功能(如补肾祛毒汤、氧化苦参碱等)、诱导宿主细胞凋亡(如苦参素等)、抑制氧化应激(如2,7-二氯荧光素、木犀草素-7-O-葡萄糖苷等)和调控JAK-STAT、PI3K-Akt-mTOR等细胞信号通路(如甜菜碱、板蓝根多糖、双氢青蒿素等)等机制。
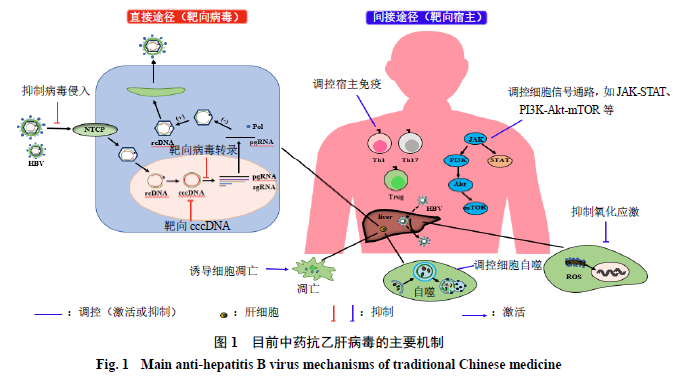
3.1 直接途径
3.1.1 抑制乙肝病毒的侵入 乙肝病毒吸附进入肝细胞是乙肝病毒生命周期中的初始环节。乙肝病毒感染进入肝细胞需要宿主肝细胞膜上钠-牛磺胆酸共转运多肽(Na+-taurocholate cotransporting poly- peptide,NTCP)和网格蛋白的参与[38-39]。因此,NTCP和网格蛋白常被作为研究乙肝病毒侵入抑制剂的靶点。Huang等[40]应用乙肝病毒感染的Hus-E/2细胞和转染HA-NTCP表达质粒的Huh7细胞,发现表没食子儿茶素没食子酸酯(EGCG)诱导NTCP从胞膜向胞质转移,继而促进溶酶体对NTCP的降解,从而抑制乙肝病毒侵入肝细胞,这可能与EGCG影响网格蛋白介导的NTCP内吞作用有关。Umetsu等[41]研究发现乳蓟提取物水飞蓟宾减少HepG2-NTCP-C4细胞中转铁蛋白的摄取,并抑制网格蛋白介导的内吞作用,进而抑制乙肝病毒侵入细胞。Tsukuda等[42]报道原花色素及其类似物抑制乙肝病毒大型表面蛋白的前S1结构域与NTCP的结合,抑制乙肝病毒进入肝细胞,降低乙肝病毒感染性,且其对各种基因型的乙肝病毒都有抑制活性。
3.1.2 靶向乙肝病毒cccDNA 乙肝病毒cccDNA的持续稳定存在是慢性乙肝患者难以治愈的主要原因之一。因此,cccDNA是研究抗乙肝病毒药物的重要靶点[43-45]。Liu等[46]建立以细胞为基础的cccDNA积累和稳定性实验,发现安石榴苷等3种可水解鞣酸能够通过抑制cccDNA形成、促进cccDNA降解降低cccDNA水平而起到抗乙肝病毒效果。Wei等[47]研究发现,从姜黄等姜科、天南星科植物中提取出的姜黄素能够显著降低cccDNA结合的组蛋白H3和H4的乙酰化水平,破坏cccDNA稳态,提示其可作为开发靶向cccDNA的抗乙肝病毒潜在化合物。
3.1.3 抑制乙肝病毒转录 高抗原负载是引发慢性乙肝患者肝损害的一个重要原因,通过抑制cccDNA转录出各种病毒RNA,从而减少乙肝病毒HBsAg、HBcAg、HBx等的表达,能够有效地缓解慢性乙肝患者体内的肝细胞损伤[48]。Pan等[49]研究发现柴胡皂苷C通过刺激IL-6表达来下调HNF-1α和HNF-4α水平,从而抑制乙肝病毒pgRNA的合成,且其对野生型和耐药性乙肝病毒均有效果。Huang等[50]报道黄芩苷亦可通过下调HNF-1α和-4α的表达来发挥抑制乙肝病毒转录及复制的作用。Bai等[51]研究表明木犀草素能激活ERK信号转导从而抑制HNF-4α的表达及其与乙肝病毒启动子的结合,进而干扰乙肝病毒的转录和复制。
3.2 间接途径
3.2.1 调控乙肝病毒诱导的细胞自噬 细胞自噬对于乙肝病毒感染的作用具有两面性:在慢性乙肝病毒感染早期,乙肝病毒可以通过诱导宿主细胞发生不完全自噬激活自身复制;而在慢性乙肝病毒感染恶化成肝癌后,细胞自噬的激活又可以通过诱导细胞死亡及增强抗肿瘤免疫反应减缓肿瘤的进一步恶化[52-53]。Zhong等[54]报道,从绿茶中提取出的多酚类化合物表没食子儿茶素没食子酸酯(epigallocatechingallate,EGCG)能够通过增强溶酶体酸化作用来抑制乙肝病毒所诱导的宿主细胞不完全自噬,从而降低宿主肝细胞内的病毒复制水平。Pant等[55]研究发现矿物沥青的主要成分腐殖酸能有效抑制HepG2.2.15细胞中HBx表达,使乙肝病毒诱导形成的自噬体减少,乙肝病毒复制水平降低。
3.2.2 调控宿主免疫功能 乙肝病毒持续感染人体后能使得全身固有免疫细胞数量减少且功能减弱,导致宿主全身固有免疫耐受;同时,由于长时间暴露于抗原高负载的肝脏环境中,宿主体内的乙肝病毒特异性T细胞功能逐渐丧失,无法有效地清除体内的乙肝病毒[56-58]。Liu等[59]报道,补肾祛毒汤通过增加Th1细胞的生成或在增加Th1细胞功能的同时抑制Th17细胞的功能来调节免疫功能,起到抗乙肝病毒的作用。Yao等[60]研究发现氧化苦参碱可以增强Toll样受体(TLR)-9信号转导分子的表达,并激活TLR9信号通路功能,诱导IFN-α和-γ等抗病毒细胞因子的产生。
3.2.3 调控宿主细胞凋亡 虽然有文献报道乙肝病毒能诱导肝细胞凋亡,但大部分学者认为乙肝病毒能够通过抑制细胞凋亡减弱机体对其清除作用[61-63]。刘欣等[64]报道苦参素可以诱导HepG 2.2.15细胞凋亡,增加S期细胞比率,进而发挥抗乙肝病毒作用。Su等[65]研究发现从方格星虫体内提取出的水溶性多糖可通过促进TNF-α、半胱氨酸-天冬氨酸蛋白酶3(cystein-asparateprotease-3,Caspase-3)等凋亡相关蛋白的表达来诱导HepG2.2.15细胞发生剂量相关性凋亡,进而抑制HepG2.2.15细胞的乙肝病毒DNA复制。
3.2.4 调控乙肝病毒诱导的氧化应激 PreS/S基因突变的乙肝病毒在宿主肝细胞内表面蛋白合成过度并积聚于内质网上,引发内质网应激,从而导致肝细胞DNA氧化损伤、基因组不稳定,进而诱发肝细胞损伤[66-67]。Arbab等[68]报道,药用植物Guiera senegalensis J.F. Gmel叶提取物能改善2,7-二氯荧光素诱导的肝细胞氧化应激,从而保护肝细胞,为潜在抗乙肝病毒活性化合物。Cui等[69]研究发现,莴苣提取物木犀草素-7-O-葡萄糖苷可能通过抑制乙肝病毒诱导的活性氧生成以改善线粒体功能来抑制HBsAg、HBeAg的分泌及乙肝病毒的转录和复制。
3.2.5 调控细胞信号通路 常见的细胞信号通路如JAK-STAT、NF-κB、PI3K-Akt-mTOR、MAPK等均与乙肝病毒复制、感染或其诱导的肝癌恶化密切相关[70-73]。中药活性提取物抗乙肝病毒作用往往涉及到多条信号通路的调控。如甜菜碱和板蓝根多糖通过增强JAK-STAT信号转导改善HepG2.2.15细胞干扰素应答反应,显示出良好抗乙肝病毒活性[74-75]。Hesari等[76]研究发现姜黄素具有抗乙肝病毒活性,作用机制与其下调NF-κB和Wnt/β-catenin信号通路有关。Zou等[77]研究发现,双氢青蒿素通过抑制三肽基肽酶I(tripeptidyl peptidase I,TPP I)表达、增强DNA损伤反应通路诱导HepG2.2.15细胞衰老及下调由Akt-mTOR信号通路诱导的HepG2.2.15细胞自噬等机制来发挥抑制HepG2.2.15细胞增殖及迁移的作用,并降低细胞在小鼠体内的致瘤性。Fang等[78]报道香菇多糖能促进单核/巨噬细胞中IL-1β、IL-12、TNF-α等细胞因子的分泌来缓解HBsAg诱导的宿主免疫功能损伤,机制可能与香菇多糖促进IκB-α磷酸化激活NF-κB信号及激活MAPK信号通路有关。Wang等[79]则报道EGCG通过激活增强ERK信号转导介导HNF-4α的表达下调,致使C/preS启动子活性下降,从而影响乙肝病毒转录和复制。
4 总结与展望
近年来,国内外研究者开展了大量的基础研究和临床试验以阐明中药提取物及复方的抗乙肝病毒疗效。茵陈、虎杖、丹参、苦参、芦荟等单味中药中的抗乙肝病毒有效成分(或提取物)陆续被文献所报道;抗乙肝病毒中药复方,以叶下珠复方、小柴胡汤、补肾复方、扶正化瘀胶囊等报道较多;报道的活性提取物及复方普遍能降低HepG2.2.15细胞培养上清、鸭乙肝病毒鸭乙肝模型或慢性乙肝患者血清中的HBsAg、HBeAg水平,部分中药甚至对乙肝病毒核苷类似物突变株也有效;另外,一些中药或提取物的抗乙肝病毒作用机制也相继被研究发现,包括抑制乙肝病毒侵入、转录、靶向cccDNA等直接途径和调控乙肝病毒诱导的细胞自噬、宿主免疫功能、宿主细胞凋亡、乙肝病毒诱导的氧化应激以及细胞信号通路等间接途径。
中药应用于乙肝病毒感染的防治显示出广阔的应用前景。然而,目前抗乙肝病毒中药的研发尚存在以下问题:(1)中药尚缺乏规范的质量标准[80],且乙肝病程的不同致使中药药效作用差异较大;(2)在抗乙肝病毒中药的临床研究中,开展的随机双盲对照试验研究较少;多数研究仅进行了中药短期疗效的评价,且大多缺乏确切的药物不良反应报告[81];(3)中药多成分、多靶点、多途径的特点给抗乙肝病毒中药作用靶点和机制的研究增添了难度[82-83]。因此,今后,应当制定统一、完善的中药质量标准,同时应用现代分子生物学技术定量患者血清中的HBsAg水平,确保中药对处于不同感染自然史阶段以及不同基因型乙肝患者的疗效稳定,实现个体化的抗病毒治疗;需要开展多中心、大规模、前瞻性、随机双盲对照试验,并进行慢性乙肝患者的长期随访研究,以获取更可靠的药物疗效数据和不良反应信息;基于中药的有效成分、分子靶点、乙肝病毒生命周期等信息,运用网络药理学分析高效预测抗乙肝病毒中药的潜在靶标。此外,在继承传统中医药理论的基础上,开展中药学与医学、药理学、药动学、病理学、生物化学、结构生物学、生物信息学、基因组学等多学科的深度融合研究,并推进基础研究与临床应用的紧密结合与协同发展,为从中药中挖掘低毒高效的抗乙肝病毒新药奠定坚实的基础。
扫二维码用手机看




